新聞資訊
新聞資訊
- 科芯微流與四川鴻鵬簽署戰略合作協議,共推微反應技術創新應用
- 動態管式反應器特點有哪些?動態管式反應器特點分析
- 哈氏合金材質微通道反應器優缺點,哈氏合金材質微反應器優缺點分析
- 連續流工藝開發有哪些步驟?連續流工藝開步驟
- 光催化連續流反應器類型有哪些?光催化連續流反應器類型
聯系我們
微化知識
羰基-光氧化還原/過渡金屬雙催化研究進展
- 作者:科芯微流
- 發布時間:2023-09-22
- 點擊:4441
摘要:
羰基-光氧化還原/雙金屬催化的有機轉化近年來備受關注。豐富且廉價的羰基光敏劑可有效地用作單電子、能量或氫原子轉移劑,以誘導金屬催化的烯烴交叉偶聯和雙官能化。本文綜述了2020年至2023年金屬催化劑參與的光催化偶聯反應的文獻報道,重點是C-C (C(sp3)-C(sp3),C(sp3)-C(sp2),C(sp2)-C(sp2), C(sp2)-C(sp))和C-雜原子(C(sp3)-S,C(sp3)-N,C(sp2)-O, C(sp2)-S,C(sp2)-P, C(sp2)-B)的成鍵反應。
Abstract:
Organic transformations using carbonyl-photoredox/metal dual catalysis have attracted much attention in recent years. Abundant and inexpensive carbonyl photosensitizers effectively serve as single electron, energy or hydrogen atom transfer agents to induce metal-catalyzed cross-coupling and dicarbofunctionalization of olefins. This review covers literature reports of metal-catalyzed photocatalytic coupling reactions from 2020 to mid-2023, with a focus on C-C (C(sp3)-C(sp3),C(sp3)-C(sp2),C(sp2)-C(sp2), C(sp2)-C(sp)) and C-heteroatom (C(sp3)-S,C(sp3)-N,C(sp2)-O, C(sp2)-S,C(sp2)-P, C(sp2)-B)bond forming reactions.
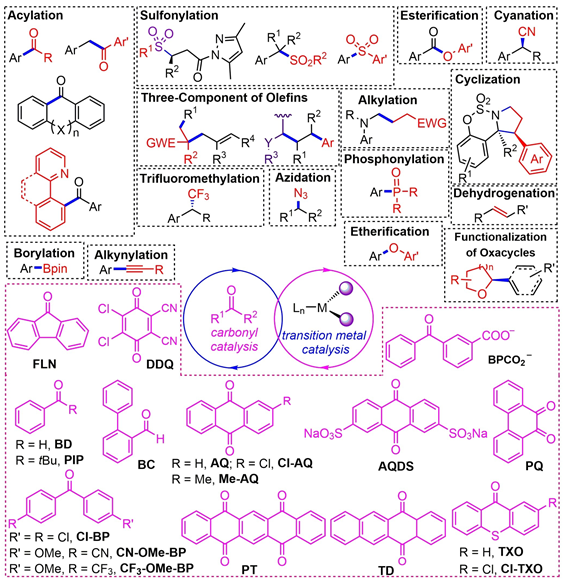
1.引言
近年來,由于MacMillan,Xiao,Molander及其同事等人的開創性研究,光氧化還原/過渡雙金屬催化已經成為促進C-C和C-雜原子成鍵的強效而又溫和的合成策略。這項工作的靈感來自釕基(Ru)和銥基(Ir)的光氧化還原催化反應。然而,由于Ru和Ir價格昂貴,低成本,低毒性的有機染料的反應范圍又比較局限。使得開發具有廣泛氧化還原能力且易于合成的廉價的有機光催化劑是非常有前景的。
芳香羰基光催化劑因其相對較低的成本、易于獲得和易于結構操作而得到了廣泛的研究。在光照射下,由非鍵合軌道(n,π*)激發電子,然后進行系間竄躍(ISC)產生長壽命三重激發態羰基,以促進氫原子轉移(HAT),單電子轉移(SET)和能量轉移(EnT)(圖1)。因為羰基自由基具有較高的鍵解離能(BDE),并且羰基的激發態具有相對較高的氧化電位和三重態能,所以實現的可能性較大。
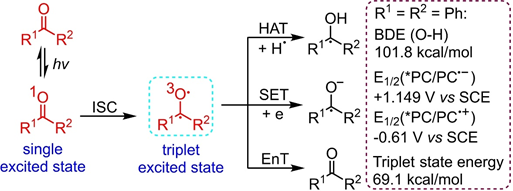
圖1 羰基的激發
本文綜述了2020年至2023年的文獻報道,詳細總結了羰基-光催化與過渡金屬催化在有機合成中的結合。按有機反應類型排列,并詳細說明每種方法的范圍、局限性和機理。
2.酰化
使用α-氧代羧酸或醛作為酰化資源,通過金屬催化活化C?H鍵實現芳烴的酰化,是形成芳基酮的一種有效合成方法。然而,這類反應需要較高的溫度或過量的氧化劑。最近,在光照條件下通過光催化產生酰基自由基,已被確定為芳烴酰化得到芳基酮更加溫和的替代圖。
2.1.醛類酰化試劑
2020年,Zheng及其同事提出了一種Pd催化的醛C?H鍵直接芳基化和烯烴化方法,以蒽醌(AQ)為HAT光催化劑得到一系列酮(圖2)。其中,溴苯與多種烷基醛的交叉偶聯反應收率良好。4-甲氧基苯甲醛是一種相容的底物,但收率較低。對于具有一系列官能團(包括富電子基團和缺電子基團)的芳基溴被容納在該系統中。其中,2-溴萘和雜芳族溴的收率令人滿意。此外,二萜藥物分子也提供了預期的酰化產物,收率為62%。
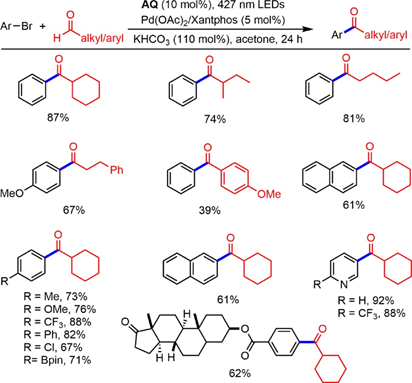
圖2 直接醛C?H芳基化和烯基化通過合并AQ和鈀催化合成酮
密度泛函理論計算表明,該光催化反應包括芳基鹵的氧化加成、捕集酰基自由基以及Pd0催化劑和AQ再生還原消除。如圖3所示,AQ(AQ*)的激發態可以轉移甲酰基氫,得到酰基自由基(2)和[AQ-H]*。PdII中間體(4),由Pd0催化劑(3)與芳基鹵化物氧化加成,捕集2得到aPdIII物種(5),然后還原消除,形成所需產物和PdI物種(6)。最后,KHCO3從6和從[AQ- H]*得到一個質子形成(3)和AQ,完成鈀催化循環和光催化循環。
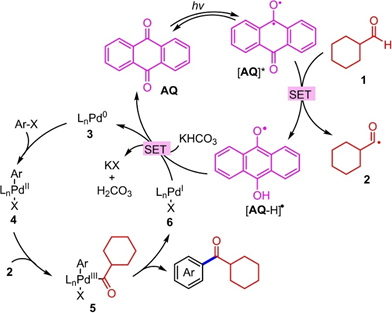
圖3 提出了AQ與Pd催化融合直接醛C?H芳基化反應的機理
隨后,Xia的小組報告了醛和芳烴偶聯的酰化圖,涉及菲醌(PQ)和鈀催化的組合,使用氧化劑Ag2O,在藍光LED照射下(圖4)。以2-苯基吡啶為反應伙伴,將各種取代的苯甲醛順利轉化為目標產物。1-萘甲醛相容,使預期產物的收率為87%。噻吩- 3 -甲醛是該反應的合適的偶聯試劑,使芳基酮的產率為81%。當使用脂肪族醛作為底物時,得到中等的產率。2-苯基吡啶類衍生物具有Me、OMe和Br基團的產物有54-88%的產率。在苯基環的對位處用含醛基、甲氧基或苯基的醛處理苯并[h]喹啉衍生物,以中等收率得到了所需的偶聯產物。
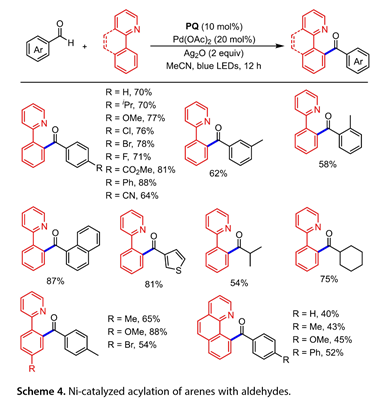
圖4. 鎳催化芳烴與醛的酰化反應
Stern-Volmer淬滅和自由基捕獲實驗表明,光催化劑與醛之間通過HAT過程生成酰基自由基。基于這些結果,提出了芳烴酰化反應的合理機制(圖5)。PQ(PQ*)的激發態可以從醛(7)中提取一個氫,從而獲得酰基自由基(8)和[PQ H]*。然后,[PQ H]*和Ag2O之間的單個電子轉移再生光催化劑。同時,由2-苯基吡啶與Pd(OAc)2反應生成的PdII配合物(9)與酰基自由基反應,然后與Ag2O結合完成(ppy)PdIV(OAc)2(TolCO)中間體(10)氧化。最后,還原消除(10)得到所需的產品和Pd(OAc)2。
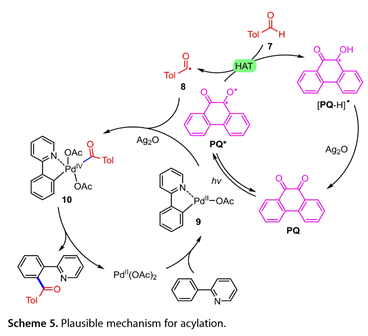
圖5. 可能的酰化機制
最近,Wu小組報道了一種新方法,該方法在Co(dmgH)2pyCl(5mol%; dmgH=二甲基乙二醛肟; py=吡啶)存在下,在二氯甲烷(DCM)中,在360nm光下反應24h (圖6),通過醛的直接激發得到一系列取代的芴酮,而無需添加光催化劑。當芳環被替換為C-4'位置的給電子基團或吸電子基團。間位二取代的[1,1'-聯苯]-2-甲醛以1:1.2的比例生產出兩種異構環化產物的混合物,總收率為86%。2'-(三氟甲基)-[1,1'-聯苯]-2-甲醛也得到了34%的成品。這種光催化反應耐受雜環芳烴,盡管產率為25%。氧雜蒽酮和硫雜蒽酮衍生物可以在這種最佳反應條件下生成,同樣具有中等產率。
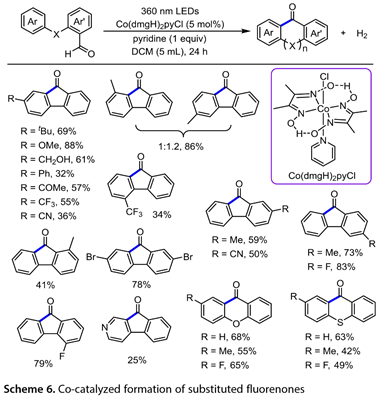
圖6. Co催化取代芴酮的形成
電子順磁共振和自由基消除實驗表明該反應中產生了甲酰基自由基。動力學同位素效應測量表明,C鍵切割不能決定速率。提出的機理(圖7)涉及360 nm光照射生成[1,1'-聯苯]-2-甲醛在激發態(11)中,從而減少Co(III)配合物以產生自由基陽離子(12)和Co(II)中間體。然后(12)失去一個質子以傳遞酰基自由基(13),該自由基可以與芳烴進行分子內自由基加成以得到(14)。然后,Co(II)中間體可以捕獲(14),以提供C-Co(III)物種(15)。β-H消除(15)產生所需的芴酮。
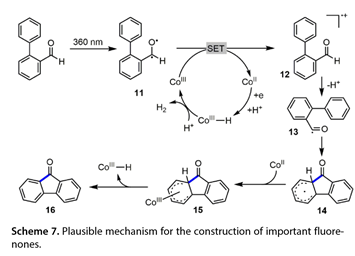
圖7. 為構建重要的芴酮類化合物提供了可能的機理
2.2. α-酮酸作為酰化試劑
α-酮酸也已通過相應的羧酸鹽和光催化劑之間的SET用于自酰化試劑[17]。在45W緊湊型熒光燈(CFL)的照射下,通過2-氯硫雜環-9-酮(Cl TXO)和鎳催化劑的組合,將α-酮酸和芳基鹵化物脫羧交叉偶聯制備了多種酮(圖8)。帶有吸電子基團的芳基溴與苯乙醛酸的反應導致脫羧芳基化產物的形成。2-溴萘也經歷了這種轉變。雜芳基鹵化物1-(6-溴吡啶-2-基)-乙基-1-酮耐受性良好,收率為80%。此外,包括取代苯基乙醛酸、脂肪族酮和2-(呋喃-2-基)-2-氧代乙酸在內的一系列α-氧代酸是該反應的合適底物,產物的產率為44-93%。據指出,缺電子的芳基碘化物比相應的芳基溴具有更高的反應活性。
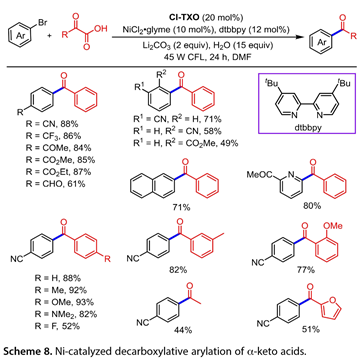
圖8. 鎳催化α -酮酸的脫羧芳基化反應
光催化活性與光催化劑的激發態氧化電位有關(圖9)。Stern-Volmer淬滅和自由基捕獲實驗表明,SET從α-酮酸到Cl-TXO*是可能的,并證實了異丙酰自由基中間體的生成。
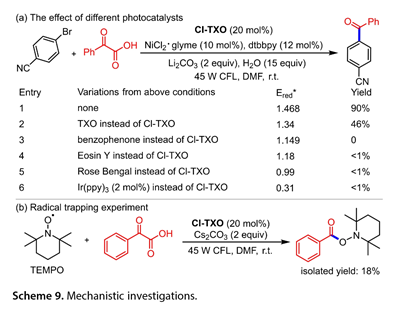
圖9. 機理研究
圖10概述了所提出的反應途徑。Cl-TXO(Cl-TXO*)和α-氧代酸的激發態之間可能發生SET,產生羧基自由基(RCOCO2*)和酮基自由基陰離子[Cl-TXO]*。前者可以釋放CO2以產生酰基自由基(RCO*,17),然后被LnNiII(Ar)X(19)捕獲,LnNiII(Ar)X(19)由ArX氧化加成LnNi0(溶劑)(18)產生,生成Ni(III)中間體LnNiIII(Ar)(RCO)X(20)。隨后,(20)進行還原消除以產生所需的酮和LnNiIX(21)。最后,介于(21)和[Cl-TXO]*之間的SET關閉循環,再生催化劑Cl-TXO和(18)。此外,Cl-TXO可用作α-氧代羧酸與烯烴脫羧交聯的高效光氧化還原催化劑,以產生多種酮(圖11)。在芳環上含有不同官能團的2-芳基乙醛酸也顯示出良好的反應活性。各種α,β-不飽和酮不適合作為該轉化的底物。
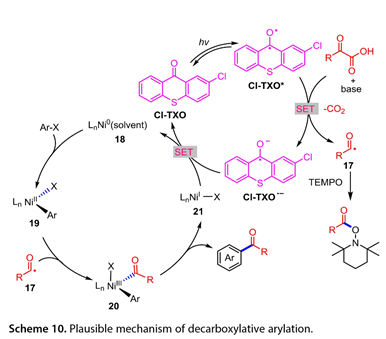
圖10. 脫羧芳基化的可能機理
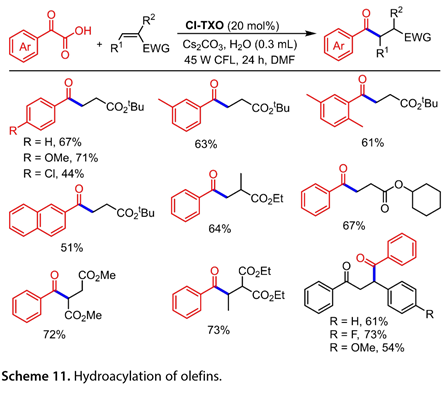
圖11. 烯烴的氫酰化反應
激發后,光激發的Cl-TXO(Cl-TXO*)氧化脫羧酸鹽α-酮羧酸鹽以生成酰基自由基(17)和酮基自由基陰離子[Cl-TXO]*(圖12)。加入酰基自由基托烯烴生成烷基自由基(22)。從[Cl-TXO]*到中間體(23)的SET然后是原生化,提供所需的產物并再生Cl-TXO光催化劑。
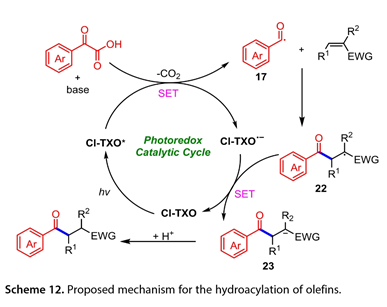
圖12. 烯烴氫酰化反應的機理
2.3. N-酰基琥珀酰亞胺作為酰化試劑
2021年,羅和他的同事報道了一種通過N-酰基琥珀酰亞胺和甲基苯的交叉偶聯合成芳香族酮的有效方法。在20W 365 nm LED照射下,將4,4'-二氯二苯甲酮(Cl-BP)(20 mol%)、NiCl2·glyme(5mol%)、dtbbpy(5mol%)、2,6-二甲基吡啶(2equiv)和甲苯及其衍生物(5mL)的混合物攪拌12h,各種N-酰基琥珀酰亞胺與甲基苯衍生物反應來得到所需產物(圖13)。甲苯與N-酰基琥珀酰亞胺在苯基環的對位上反應,形成偶聯產物(產率為56-72%)。缺電子的N-酰基琥珀酰亞胺耐受性良好,盡管產量較低。空間位阻效應影響了轉化,獲得了48-67%的產率。甲苯處理1-(3-苯基丙酰基)-吡咯烷-2,5-二酮得到C(sp3)鹵化產物,收率38%。此外,對二甲苯或間二甲苯與N-酰基琥珀酰亞胺的反應得到64-70%的產率,但鄰二甲苯的產率為18%,這表明空間位阻減緩了反應速率。對氯甲苯和乙苯也提供了34-40%的預期產品產率。當對二甲苯與Me取代的N-酰基琥珀酰亞胺偶聯時,獲得了良好的收率。
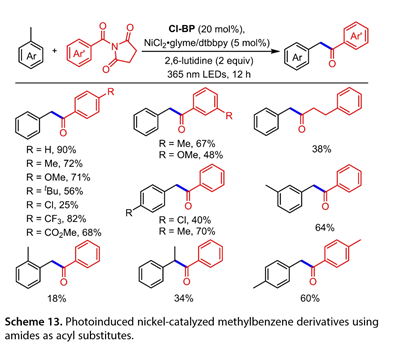
圖13. 以酰胺為酰基取代基的光誘導鎳催化的甲苯衍生物
當甲苯和Cl-BP的混合物被365 nm LED照射12小時(圖14)時,觀察到1,2-二苯基乙烷,表明形成了[Cl-BP-H]*。添加自由基清除劑2,2,6,6-四甲基-1-哌啶-氧基(TEMPO)可以有效地抑制這種反應。這些結果表明,該光催化反應中產生了芐基自由基。圖15概述了可能的機制。用20W 365 nm LED 照射Cl-BP得到激發的Cl-BP(Cl-BP*),它可以從甲苯中提取氫以得到[Cl-BP-H]*和芐基自由基(24)。同時,N-酰基琥珀酰亞胺衍生物(25)氧化加成LnNi0(26)生成中間體(27)。隨后,(24)與(27)結合以遞送NiIII (28)。還原消除得到所需的芳香族酮和(29),隨后通過[Cl-BP-H]*還原得到Cl-BP和(26),從而完成該催化循環。
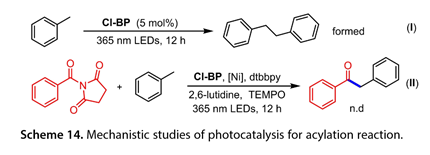
圖14. 光催化酰化反應的機理研究
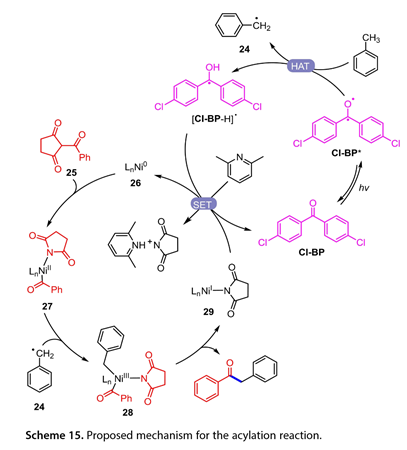
圖15. 推測的酰化反應機理
3. 芐基C-H的三氟甲基化
2022年,Liu及其同事報告了通過光氧化還原和不對稱銅催化組合的芐基C-H鍵的首次對映選擇性自由基三氟甲基化(圖16)。在395 nm LED 的照射下,使用 Cu(MeCN)4PF6(15 mol%)、L1(18 mol%)、2-氯蒽-9,10-二酮(Cl-AQ,10mol%)和并四苯- 5,12 -二酮(TD,4mol%)在 CHCl3中成功進行了一系列對映選擇性芐基C-H三氟甲基化。在3位或4位的乙苯取代基以58–78% 的產率和出色的對映選擇性 (82–94% ee)得到產物。此外,烷基碳鏈上的一系列官能團,如鹵素、酯、酰胺和砜,耐受率為48-77%,ee為85-91%。雜芳烴,包括苯并[d]噻唑和苯并[d]惡唑,成功地與Togni-II偶聯,提供了53-62%的產率和92%ee的所需產物。使用這種雙重催化體系進行區域選擇性C-H三氟甲基化反應提供了合理的產率(41-61%)和出色的對映選擇性(88-94% ee)。

圖16. 加入鎳催化芐基碳氫鍵三氟甲基化反應
Stern-Volmer熒光猝滅實驗表明,該襯底可以有效猝滅光催化劑的激發態。動力學同位素效應測量表明,該反應的速率決定步驟是HAT過程。降低反應溫度提高了反應收率和對映選擇性。該結果證明差異焓有助于對映決定步驟。如圖17所示,AQ最初由395 nm LED激發,以產生激發的AQ(AQ*)。然后,自由基AQ*可以從乙苯的芐基位置提取氫,提供芐基自由基(30)和[AQ-H]*。同時,將L*Cu(I)(31)被Togni-II試劑氧化得到L*(OBz')Cu(III)CF3(32),經[AQ-H]*還原,得到L*Cu(II) CF3(33),AQ再生。最后,L*Cu(II)CF3物種可以捕獲30,導致目標產物的形成,從而完成催化循環。
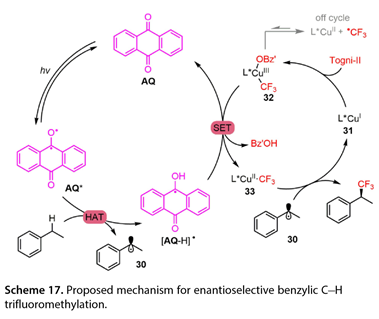
圖17.對映選擇性芐位C-H三氟甲基化反應機理
4.環合反應
2022年,Gong及其同事報告了一種光催化非對映和對映選擇性分子內環化反應的方法(圖18)。455 nm LED、5,7,12,14-戊烯醚酮(PT)(5mol%)、L2(11mol%)、NiBr2(10 mol%)、Na2CO3(1.5eq)在CHCl3中照射。有效地促進了這種立體選擇性C(sp3)功能化/環化級聯反應。在苯基環的對位帶有吸電子基團或供電子基團的(3-氯丙基)-苯轉化為所需的手性多環苯并磺胺(42-82%產率,高達>20:1dr,52-98% ee)。用N-磺酰胺處理2-(3-氯丙基)-噻吩也導致多環產物的形成。然而,這種光催化反應不適用于仲氯化物和叔氯化物。在優化條件下耐受各種N-磺酰亞胺,產量不適中,ee為80-92%,最高可達20:1dr。
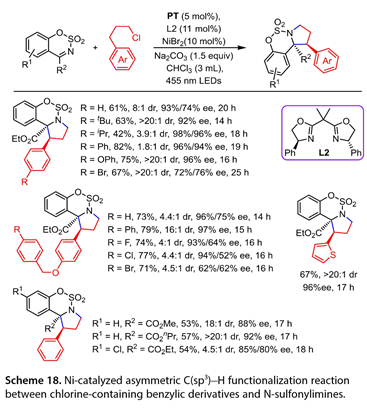
圖18. Ni催化含氯芐基衍生物與N -磺酰亞胺的不對稱C ( sp3 ) H官能化反應
在優化的反應條件下,1-(氯甲基)-2-甲基苯、2(氯甲基)-1,3-二甲基苯和4-溴-1(氯甲基)-2-甲基苯與N-磺酰亞胺反應,得到的相應產物收率51–68%,ee為76–91%。具有兩個鄰近立體中心的手性稠合四氫異喹啉的產率為64–76%,ee為91–99%(圖19)。

圖19. Ni催化的手性四氫異喹啉類化合物的制備
該反應的擬議機理如圖20所示。PT通過輻照激發產生激發物種PT*。PT*提取(3氯丙基)-苯的芐基C-H鍵得到C中心自由基(34)和[PT-H]*,進而還原鎳配位的N-磺酰亞胺(36)生成中間體(37)和光催化劑(PT)。中間體38由34加入到37形成,然后分子內親核攻擊得到39。隨后,中間體39和35之間的配體交換產生目標產物和中間體36,從而完成催化循環。
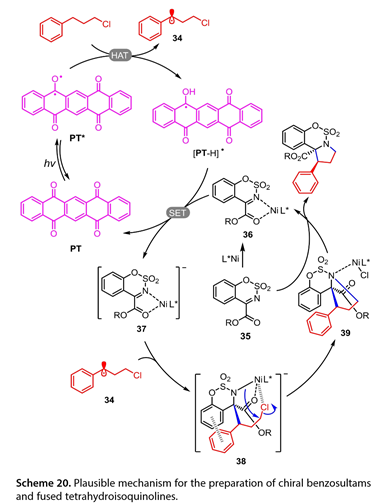
圖20. 可能的機理用于制備手性苯并磺內酰胺和四氫異喹啉類化合物
5.芳基鹵化物的炔化反應
2020年,Liand及其同事[21]利用噻噻烷-9-酮(TXO)作為光敏劑,在45W CFL的照射下,以無水Zn(OTf)2為添加劑,有效地加速了炔烴的芳基化反應(圖21)。含缺電子基團和富電子基團的芳基炔烴成功地偶聯到4-溴苯腈上,產率良好至中等(產率為68-93%)。2-乙炔基萘參與了這一轉化,收率為62%。4-乙炔基吡啶也可用作底物,得到相應產物的收率為55%。烷基炔烴反應平穩,使芳基化產物收率差至極好。與乙酮反應產生所需產品收率45%。1-乙炔基-4甲基苯與苯基環上不同官能團的芳基溴芳基化反應進展順利,收率達到49–89%。發現雜芳基溴是有效的偶聯伙伴(產率為72%)。然而,當使用5-溴苯并[d][1,3]-二惡茂時,沒有觀察到所需的產物。相比之下,5-碘苯并-[d][1,3]二惡確實反應了62%的產率。
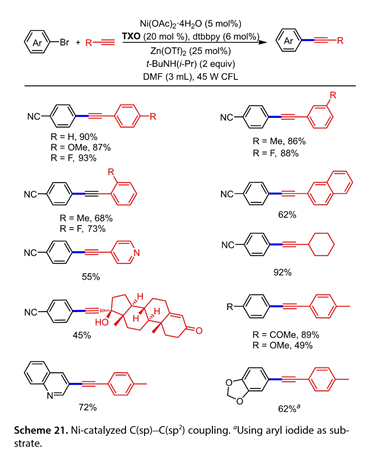
圖21. Ni催化的C(sp) C(sp2)偶聯反應。以芳基碘化物為底物
如表1所示,目標產物的產率與光催化劑的三重態能(ET)密切相關,而不是與激發態氧化電位密切相關,并且具有最高ET的TXO被證明是最有效的。用1-乙炔基-4-甲基苯處理(dtbbpy)-4-氰基苯基溴化鎳(Ni-1),在45W CFL和紫外光的照射下,分別得到13%和24%的預期產物產率(圖22)。4-溴苯腈和1-乙炔基-4-甲基苯在45W CFL或者在365 nm下交叉偶聯得到11%或16%的產物收率。這些結果表明,光催化劑激發態與NiII中間體之間的三重態-三重態能量轉移參與了該反應。
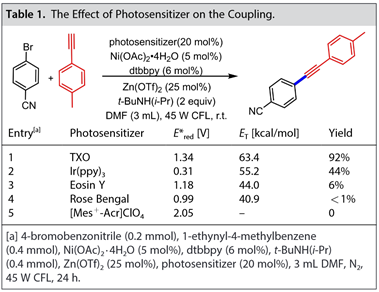
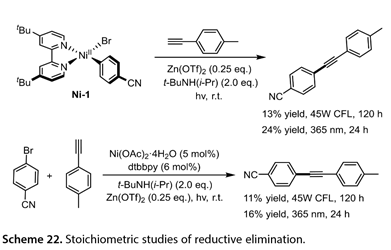
圖22. 還原消除的化學計量學研究
非機理研究揭示了退出狀態光催化劑與Ni(II)之間的初始能量轉移(圖23)。芳基鹵化物的氧化加成[(dtbbpy)Ni0](41)得到(dtbbpy)NiII(Ar)X(42)。(42)與原位形成的乙酰炔鋅(40)的金屬轉染生成芳基-Ni(II)乙酰基(43)。同時,用光照射將TXO轉換為光激發TXO(TXO*),然后將能量轉移到(43)。得到的(44),經過還原消除,得到目標產物,從而完成催化循環。
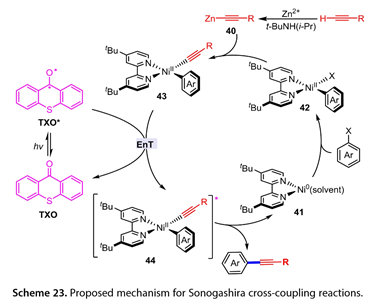
圖23. 提出的Sonogashira交叉偶聯反應機理
6.芳基鹵化物的醚化
一些研究人員報道了在可見光下使用TXO作為光敏劑對酚和芳基鹵化物進行鎳催化醚化(圖24)[22]。一系列的機理實驗表明,涉及從TXO(TXO*)激發態到NiII復合物的三重態能量轉移的過程可能是可操作的。鄰位、間位或對位取代的溴苯與苯酚高效偶聯,使聯芳基醚的產率為60-91%。當使用2-溴萘時,以51%的收率獲得所需的產物。雜芳基溴提供了相應的產品,收率為94%。觀察到在酚的3或4位存在富電子或電子中性基團有利于這種光催化反應。然而,貧電子酚需要延長120 h的反應時間,收率達到51-53%。同樣,鄰位取代的酚提供了所需的產物,但需要更長的120小時照射時間。值得注意的是,氯代芳烴,1 - ( 4 -氯苯基)-乙酮,也能以28 %的產率得到。
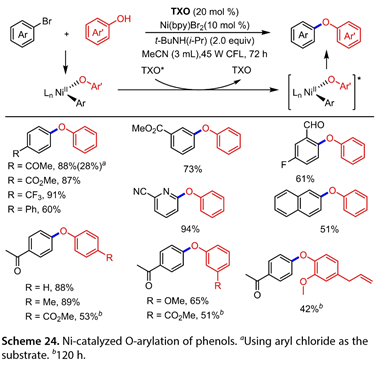
圖24. Ni催化苯酚的O -芳基化反應。以氯代芳烴為底物
7.酚類酯化反應
2022年,Li和合作者[23]報道了一種通過Ni催化的苯酚與芳香醛的無受體脫氫酰基化反應合成苯甲酸芳酯的新方法( 圖 25 )。值得注意的是,這種光催化反應不需要外部光催化劑,因為醛執行了這種作用。在NiCl2 glyme ( 10mol %),dtbbpy ( 12mol %),Na2CO3 ( 1equiv )存在下,以二氯乙烷( DCE , 1mL)為溶劑,365 nm LEDs下反應24h,成功實現了醛與酚的偶聯。值得注意的是,戊醛與保護的α -氨基在20mol %的苯甲醛催化下,以70 %的產率得到了偶聯產物。雌酮是該光催化反應的良好底物,在最優條件下,偶聯產物的產率為85 %。
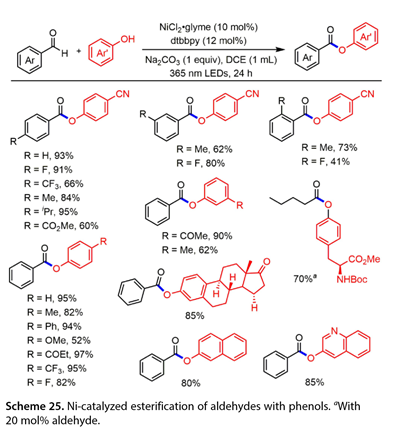
圖25. 鎳催化的醛與酚的酯化反應
熒光猝滅實驗表明苯甲醛( BD * )的激發態與苯酚或酚酸鹽之間存在一個SET過程。在優化的反應條件下,加入1,1 -二苯基乙烯或2,6 -二叔丁基- 4 -甲基苯酚作為自由基捕獲劑,分別得到了2 %和15 %的目標產物,表明酰基自由基的存在生成。高分辨質譜( HRMS )表明苯氧基、羥苯基和苯甲酰基的產生。在(圖26)中概述了醛與酚酯化反應的可能機理。用365 nm的LED照射BD,得到激發的BD *。芳氧自由基( Ar ' O * , 45)可以通過酚酸鹽陰離子或苯酚與BD *之間的SET或HAT得到。BD *還可以從苯甲醛中奪取一個氫原子,得到一個苯甲酰基自由基( ArCO *、46 )和BD *。中間體(45)和(46)可與LnNiⅠ- X ( 47 )反應生成LnNiⅢ( Ar ' O) ( ArCO ) X ( 48 ),然后經過還原消除生成目標產物和(47)。生成的NiI絡合物再與Ar ' OH或H+反應,得到Ni ( II )中間體( 49 )和H2。最后用BD·-對(49)進行消除,重新生成BD和(47).
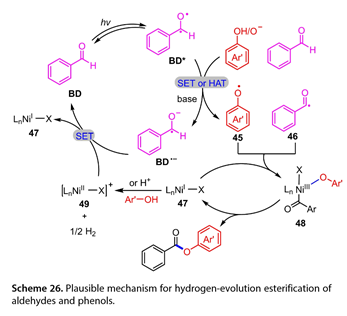
圖26. 醛、酚類化合物可能的析氫酯化反應機理
8.硼化
在2023年,Takaya和他的合作者[24]報道了通過光能和Rh催化的組合來實現芳基酮的C-C σ -鍵的硼化來合成芳基硼酸酯(圖27)。一系列苯環對位帶有給電子或吸電子基團的特戊烯酮以良好的產率得到了所需的芳基硼酸酯。然而,4 - Ph取代的特戊烯酮并不是該反應的合適底物。間位和鄰位取代的苯乙酮也被硼化,以56 ~ 81 %的收率得到預期產物。含縮酮結構的底物與HBpin反應得到了目標產物。此外,羰基碳上的一系列烷基也被接受( 16-48 %的產率)。自由基捕獲劑實驗表明,該反應涉及苯甲酰基自由基中間體。用DBpin代替HBpin進行氘標記實驗表明,氘轉移到產物異丁烷的次甲基碳上。基于這些結果,提出了一種可能的機制(圖28 )。在365 nm光照下,PIP可通過C-C σ -鍵的σ -斷裂產生芳酰基自由基( 50 )和叔丁基自由基( 51 )。(51)和HBpin之間的HAT導致異丁烷( 53 )和硼基自由基的形成。隨后,(50)與硼自由基被銠配合物( 52 )捕獲,得到芳酰基(硼基)銠配合物( 54 ),該配合物擠壓CO生成芳基(硼基)銠配合物( 55 )。最后,還原消除(55)得到硼化產物同時再生銠配合物(52),從而完成催化循環。

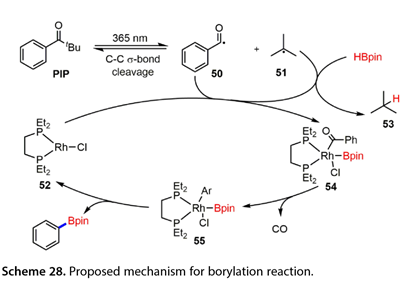
圖27和28. Rh催化C-C σ鍵斷裂合成芳基硼酸酯過程機理
9 .磺化
2021年,Gong及其合作者報道了環烷烴、烷烴、甲苯衍生物和醚的直接和選擇性不對稱磺酰化反應的有效方法(圖29 )[25]。在24W 455 nm LED照射下,以二氯乙烷為溶劑,以5,7,12,14 -五乙酰苯乙酮( PT )、L3( 18mol %)、Ni( ClO4 )2·6H2O ( 15mol %)為原料,對一系列未取代的環烷烴與1,4 -二氮雜雙環[ 2.2.2 ]辛烷1,4 -二鎓- 1,4 -二亞磺酸鹽( DABCO·( SO2 ))2和含N-酰基吡唑的α,β -不飽和羰基化合物進行磺酰化反應,以優異的化學選擇性( 91 ~ 95 % ee)得到62 ~ 73 %的收率。均三甲苯工作良好,得到相應的手性產物( 72 %收率, 90 % ee)。二級芐基烴與( DABCO·( SO2 ))2和N-酰基吡唑的反應獲得了中等收率。2 -甲基噻吩以60 %的收率得到目標產物,ee值為88 %。含有β -芳基的α,β -不飽和N-酰基吡唑也能以60 %的收率得到,83 %的ee值。
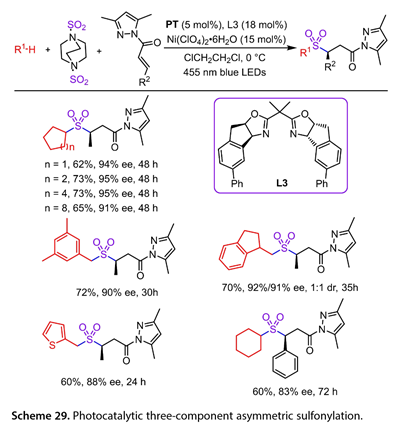
圖29. 光催化三組分不對稱磺酰化反應
TEMPO的存在完全抑制了該反應,并通過HRMS觀察到TEMPO-C自由基產物(圖30)。4 - (環丙基甲基) – 1,1 ' -聯苯反應以63 %的產率得到開環產物。此外,PT的激發態被甲苯猝滅。這些觀察與芐基自由基的形成是一致的。環丙基取代的N-酰基吡唑沒有得到開環產物,說明N-酰基吡唑的β -碳自由基不是中間體。同樣,用N-酰基吡唑處理環戊烷亞磺酸鈉也沒有得到預期的產物,排除了磺酰負離子中間體的形成。
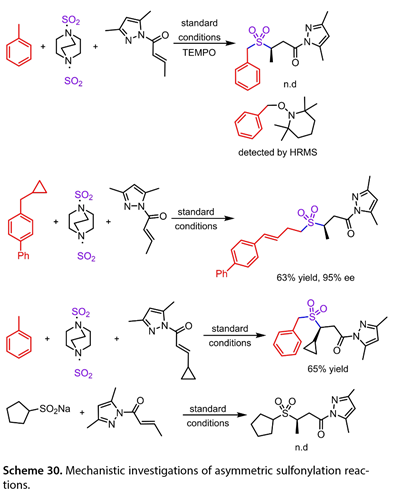
圖30. 不對稱磺酰化反應的機理研究
反應機理如式( 31 )所示。首先,在455 nm LEDs的照射下,PT被激發到三重態( PT * ),它可以從R1-H中提取一個氫原子,生成[ PT-H ] *和碳自由基中間體( 56 )。然后,二氧化硫釋放原位空穴(56),以容納磺酰基自由基( R1SO2 * ) ( 57 )。同時,α,β -不飽和N-酰基吡唑( 61 )與L * Ni進行配體交換得到Ni配合物( 58 ),配合物( 58 )可與(57)反應得到中間體(59)。(59)和[ PT-H ] *之間的單電子轉移可以產生PT和中間體(60)。隨后在中間體(60)和(61)之間進行配體交換,得到所需的手性砜,完成光催化循環。
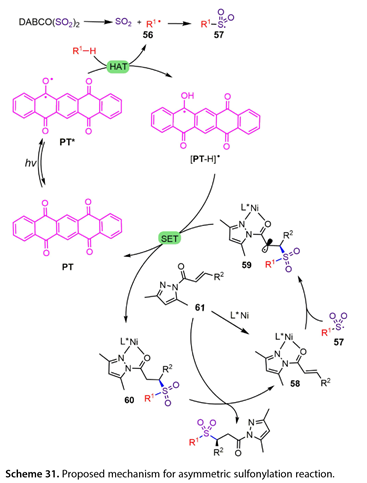
圖31. 提出了不對稱磺酰化反應的機理
最近,Gong等報道了在PT存在下,甲苯衍生物和環烷烴與亞磺酸鈉發生位點選擇性C(sp3)-H磺酰化反應的溫和方法( 10 mol % )和Cu (OTf)2 (1.2 equiv),在50 W 410 nm LED照射下(圖32)。富電子的乙苯可以有效的偶聯,以良好的產率( 64-74 % )得到目標產物。含有順式側鏈或遠程官能團的次級芐基碳氫鍵底物也能有70 - 78 %的產率。含有二級和三級C-H鍵的1 -乙基- 4 - ( 4 -異丙基苯氧基)苯與苯亞磺酸鈉反應以48 %的收率得到目標產物,位點選擇性為2:1rr。在苯環對位帶有吸電子或供電子基團的芳基磺酸鹽與交叉偶聯是相容的。噻吩- 2 -亞磺酸鈉或萘- 2 -亞磺酸鈉經此偶聯反應,以71 - 75 %的收率得到目標產物。值得注意的是,烷基亞磺酸鈉適合于這種轉化,并且在最佳反應條件下獲得了良好的產率。此外,其他C(sp3)-H前體,如環烷烴、金剛烷與4 -溴苯亞磺酸鈉的磺酰化反應也能以中等的產率得到目標產物。
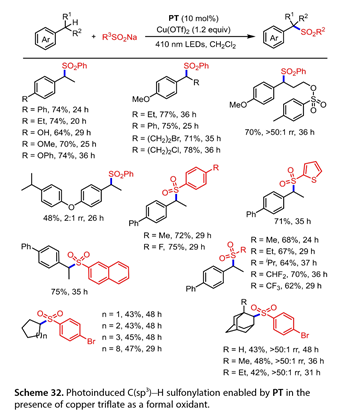
圖32. 在三氟甲磺酸銅作為氧化劑通過PT實現了光誘導的C(sp3)-H磺酰化反應
機理研究表明,激發態的PT ( PT * )可以從C(sp3)-H前體中抽提H原子,得到以C為中心的自由基( 62 )和[ PT-H ] * (圖33 )。同時,Cu ( OTf )2( 63 )與R4SO2Na反應生成[ TfO - CuⅡ- SO2R4] ( 64 ),[ TfO - CuⅡ- SO2R4] ( 64 )捕獲62得到Cu ( III ) ( 65 )。該65再經過還原消除,生成目標產物和CuIOTf。最后,CuⅠ中間體歧化生成Cu0和CuⅡ。后者再被[ PT-H ] *還原生成CuI和PT,從而完成催化循環。
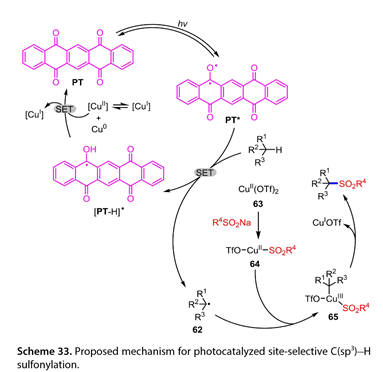
圖33. 提出了光催化反應位點選擇性C(sp3)-H磺酰化的機理
2022年,Li課題組報道了在dtbbpy ( 12 mol % )、DMSO ( 3 m L )存在下,以2 -氯-硫代氧雜蒽- 9 -酮( Cl-TXO )為光催化劑,鎳催化芳基亞磺酸鹽與(雜)芳基鹵化物的交叉偶聯反應(圖34)。文獻報道了苯亞磺酸鈉與一系列苯環4位、3位、5位帶有吸電子或供電子基團的芳基溴化物的交叉偶聯反應,得到了目標產物(收率35 % ~ 90 %)。鄰位取代的芳基溴化物以47 % ~ 53 %的收率得到交叉偶聯產物。2溴代萘與雜環芳基溴化物反應,以中等收率得到磺酰化產物( 50 ~ 88 % )。產量)。以55 - 83 %的收率分離了F、Me、CF3取代的芳基磺酸鈉。萘- 2亞磺酸酯的芳基化反應以60 %的收率得到相應的產物,雜環磺酸鈉與4 -溴苯腈反應以50 %的收率得到相應的二芳基砜。
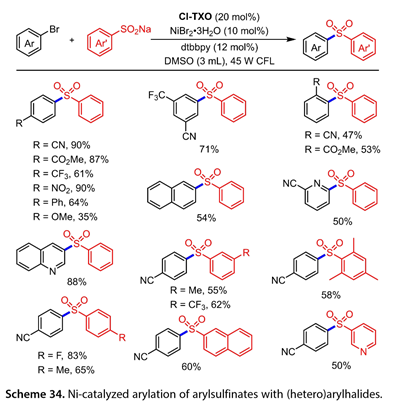
圖34. Ni催化芳基亞磺酸酯與(雜)芳基鹵化物的芳基化反應
如圖 35所示,預期產物的產率與光催化劑的激發態氧化還原電位有關,還原電位最高的Cl-TXO是最有效的,表明SET介于光催化劑和鎳催化循環之間。此外,1,1 -二苯基乙烯或TEMPO的加入導致產率降低,表明該反應有自由基物種參與。
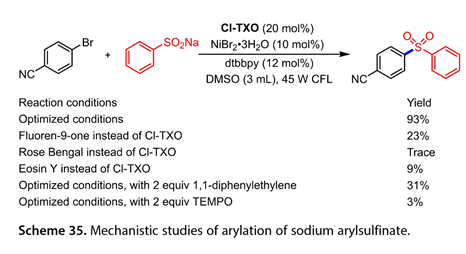
圖35. 芳基亞磺酸鈉芳基化反應的機理研究
Cl-TXO的激發態( Cl-TXO * )可以氧化Ar ' SO2Na得到[ Cl-TXO ] *和芳基磺酰基自由基( Ar ' SO2 *) ( 66 ) (圖式36 )。隨后,Ar-X與Ln Ni0(溶劑) ( 67 )氧化加成生成的Ln NiII ( Ar ) X ( 68 )捕獲(66)得到NiIII中間體( 69 )。中間體(69)經過還原消除得到所需的二芳基砜和LnNiI - X ( 70 )。最后,(70)氧化[ Cl-TXO ] *完成催化循環。
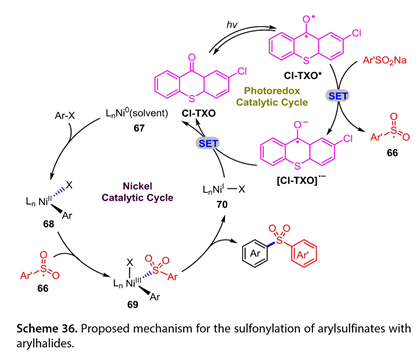
圖36. 提出了芳基亞磺酸鹽與芳基鹵化物的磺酰化反應機理
10 .芳基鹵化物的磷酸化
2021年,Li和同事報道了在45 W CFL輻照下,通過硫代氧雜蒽- 9 -酮( TXO )和鎳催化劑的組合構建芳基氧膦和芳基磷酸酯,用于H -氧膦和H -亞磷酸酯與芳基鹵化物的芳基化反應(圖37 )[28]。缺電子的溴代芳烴以中等到良好的產率發生偶聯反應,而富電子的溴代芳烴不發生反應。1 - Iodo - 4-甲基苯酚以66 %的收率得到預期產物。3溴喹啉同樣以67 %的收率得到相應的產物。一些H -膦氧化物和H -亞磷酸酯底物,如二對甲苯基氧化膦、二烷基亞磷酸酯和二苯并[ c、e][ 1、2 ]氧雜膦- 6 -氧化物,都能以較好的產率得到芳基化產物。
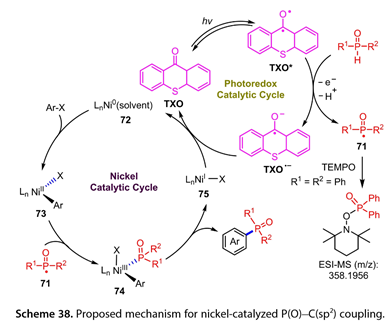
圖37. Ni催化的芳基鹵化物的光誘導膦酰化反應
產物的產率與光催化劑的激發態氧化還原電位有很強的相關性。此外,在這種光誘導膦酰化反應中產生了以磷為中心的自由基,通過電噴霧電離質譜和自由基捕獲實驗進行了表征。如圖38所示,激發態的TXO ( TXO* )與[ R1R2P ( O )H ]之間的SET或HAT過程生成[ TXO ]*和[ R1R2P (O)* ] ( 71 ),然后參與鎳催化的芳基溴化物的膦酰化反應,包括Ar-X與Ln Ni0的氧化加成( 72 ),71與Ln NiII ( Ar ) X的加成( 73 ),以及Ln NiIII ( Ar ) ( POR1R2 ) X的還原消除( 74 ),得到目標產物和Ln NiIX ( 75 )。
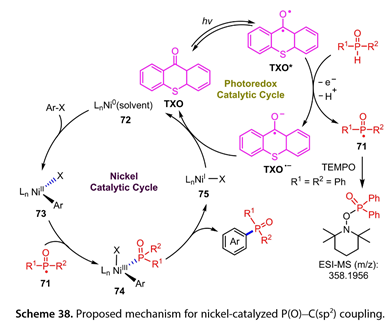
圖38. 提出了鎳催化P(O)-C(sp2)偶聯的機理
11.三組分烯烴偶聯
Wang課題組在溫和條件下發現了一種鈀催化的烯丙基烷基化反應,該反應涉及一種HAT光催化劑介導的親核試劑生成策略(圖39)。多種末端烯烴,脂肪族C ( sp3 ) H偶聯伙伴以5,7,12,14 -五苯乙酮( PT ) aHAT為光催化劑,Pd2 ( dba ) 3 / P( 3 , 5 - Me2C6H3)3為催化劑,DCE為溶劑,在6W 420 nm LEDs的照射下,烯丙基碳酸酯適合于該三組分偶聯反應。苯環上帶有給電子或吸電子取代基的末端烯烴均能以56 - 83 %的產率得到所需的烯丙基化產物。在該烯丙基烷基化反應中也引入了2 - (吡啶- 3 -基)丙烯酸甲酯,發現α -烷基丙烯酸酯是有效的,以51 - 54 %的收率得到交叉偶聯產物。同樣,烯丙酰苯也得到了目標產物( 50 %收率)。2,3 -二甲基丁烷在第3位進行官能化。吸電子基、富電子基或電子中性基取代的甲苯產品收率48 - 81 %。2 -甲基噻吩也是一個合適的底物,以42 %的產率得到了預期的產物。環己基苯的芐位選擇性C-H官能化反應以45 %的產率得到了預期的產物。1,3 -苯并二氧雜環戊烷以優異的收率( 84 % )反應。值得注意的是,一些取代的烯丙基碳酸酯,包括2 -烷基和2 -芳基取代的烯丙基碳酸酯也以61 - 80 %的產率得到了相應的產物。
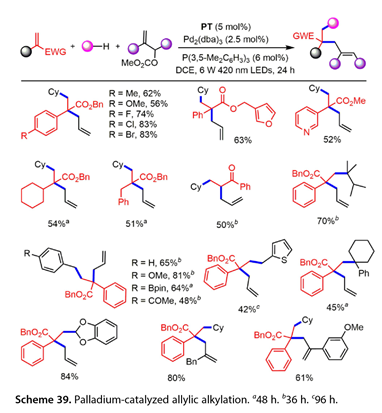
圖39. 鈀催化烯丙基烷基化反應a48h . b36h . c96h .
在模型反應中加入TEMPO有效地阻止了烯丙基烷基化反應的進行,并通過HRMS檢測到了烷基- TEMPO加合物(圖40 )。Stern – Volmer淬滅實驗表明,環己烷或甲苯降低了PT的光致發光強度。這些結果表明,激發態的PT將H原子從C H耦合伙伴中提取出來。此外,在Pd2 ( dba )3和P(3,5 - Me2C6H3)3存在下,Giese加成產物和甲基烯丙基碳酸酯的處理并沒有得到所需的烯丙基化產物,表明光催化Pd催化的烯丙基烷基化反應并沒有發生。質子轉移穿梭體六氟異丙醇( HFIP , 60mol %)的存在完全抑制了反應的進行,表明該反應涉及質子轉移。
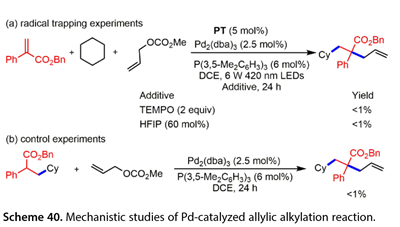
圖40. 鈀催化烯丙基烷基化反應的機理研究
在圖41中,我們提出了一種雙光氧化還原/鈀催化機制。激發態PT ( PT * )和環己烷之間的HAT導致烷基自由基( 76 )和[ PT-H ] *的形成。前者迅速被貧電子烯烴捕獲,生成缺電子自由基( 77 ),該自由基被[ PT-H ] *氧化生成碳負離子親核試劑( 78 ),PT再生。Pd0( 79 )與烯丙基碳酸酯配位,形成π -烯丙基中間體( 80 )。然后,Pd -配合物(80)失去碳酸二甲酯,得到陽離子型Pd (Ⅱ) π -烯丙基配合物( 81 )。該物種隨后受到(78)的攻擊,產生所需的產物,再生(79)。
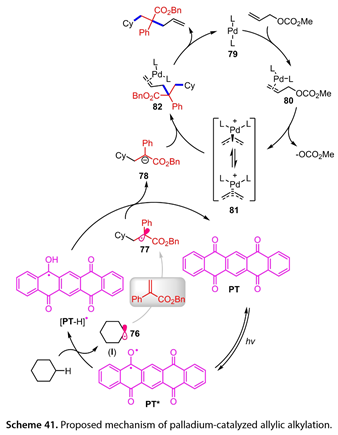
圖41. 提出了鈀催化烯丙基烷基化反應機理
2021年,莫蘭德及其合作者報道了鎳催化的以醚或醇為自由基前體,4 - ( 4 -甲氧基苯甲酰基)苯甲腈(CN-Ome-BP)為催化劑的烯烴多組分雙碳官能化反應(圖42)。Zhang等用含吸電子基團的芳基溴化物處理環戊基甲醚,得到了較好的交叉偶聯產物。電子中性或供電子的芳基溴化物不是合適的底物,但芳基碘化物具有足夠的反應活性。氟馬西尼被轉換為以36 %的收率得到目標產物。5 -溴- 2 - (三氟甲基)吡啶以65 %的收率得到相應的目標產物。醇和α -硼酸酯底物參與了該轉化,得到了目標產物(收率35 ~ 91 %)。此外,一系列內烯烴以34-80 %的收率和良好的非對映選擇性反應。
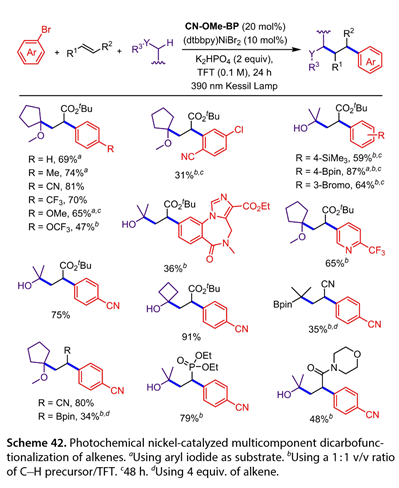
圖42. 光化學鎳催化烯烴多組分雙碳官能化反應
圖43概述了三組分HAT介導的光氧化還原/鎳雙催化烯烴雙碳官能化的機理。激發態的CN-Ome-BP ( CN-Ome-BP *)可以從C-H底物中抽提H原子得到[ CN-OMe-BP-H] *和碳中心自由基( 83 ),然后與活化的烯烴發生Giese加成,得到相應的自由基加合物( 84 )。同時,Ar-Br與Ni ( 0 )( 85 )發生氧化加成反應,生成Ni ( II )中間體( 86 ),后者捕獲(84)生成Ni ( III )配合物( 87 )。接著,(87)的還原消除得到目標產物和Ni ( I )配合物( 88 )。最后,(88)和[ CN-OMe-BP-H] *之間的SET再生CN-OMe-BP和產物(85),完成兩個催化循環。
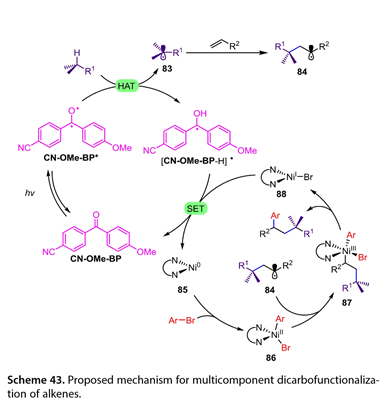
圖43. 提出了烯烴多組分雙碳官能化的機理
2022年,No?l小組[31]報道了近紫外光誘導Ni催化的二苯甲酮類光催化劑和硅烷參與的烯烴的交叉親電偶聯和1,2 -二碳官能化反應( 圖 44 )。在( 4-甲氧基苯基) ( 4- (三氟甲基) phenyl )甲酮(CF3-OME-BP),( dtbbpy ) Ni Br2,2,6-二甲基吡啶,( TMS ) 3Si H存在下,伯、仲烷基溴與對溴苯甲酸甲酯高效偶聯,在16 W 365 nm連續流動光照射下,以55 - 90 %的產率得到相應的產物。二級雜環烷基溴化物具有良好的耐受性,以50-76 %的產率得到芳基化產物。雄酮以60 %的收率得到目標產物。利用該光致發光器件將不同范圍的(雜)芳基溴化物與溴丙基硼酸頻哪醇偶合如5 -溴- 2 - (三氟甲基)吡啶、5 -溴苯并[ b ]噻吩、5 -溴- 1 -甲基- 1H -吲哚、2 -溴二苯并[ b、d]呋喃等,也有使用這種連續流動協議(收率56 ~ 76 %)對交叉耦合產品進行了研究。以Ph CF3為溶劑,在390 nm下照射16 h進行烯烴的還原1,2 -雙官能團化反應( 圖 45 )。環己基溴化物、丙烯酸叔丁酯和芳基溴化物在對位和間位引入吸電子或供電子基團,反應收率為40 % ~ 63 %。雜芳烴5 -溴- 2 (三氟甲基)吡啶也能順利反應,以45 %的產率得到目標產物。含氧和氮雜原子的雜環溴化物也被容忍,給出交叉偶聯產物的產率在45 - 56 %。無環溴化物是該轉化的適宜底物(產率65 % )。1,3 -二溴金剛烷以67 %的收率在單一位置被官能化。苯乙烯基硼酸頻哪醇酯和呋喃- 2 ( 5H )均為較好的底物,產率分別為72 %和61 %。甾酮衍生物也是良好的底物。值得注意的是,4 -取代苯甲酰氯和丁酰氯也可用于(收率42 % ~ 65 %)。
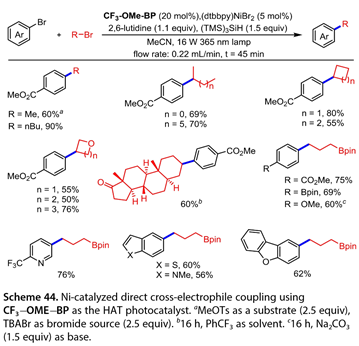
圖44. 以CF3-OME-BP為HAT光催化劑,Ni催化的直接交叉親電偶聯反應
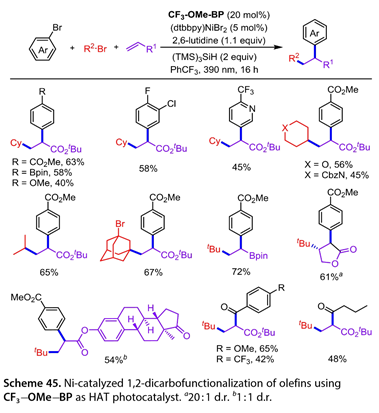
圖45. 以CF3-OME-BP為HAT光催化劑,Ni催化烯烴的1,2 -雙碳官能化反應
該還原交叉偶聯的機理涉及激發態CF3-OME-BP從( TMS )3SiH中提取氫生成硅中心自由基( 89 )和酮基自由基[CF3-OME-BP-H] * ( 圖46 )。鹵素原子從溴代烷基轉移到(89),形成( TMS )3SiBr和以碳原子為中心的自由基( 90 )。由Ar BrtoaNi ( 0 )物種( 91 )氧化加成生成的中間體(92)捕獲(90),得到( dtbbpy ) NiⅢ( R ) ( Br ) ( Ar ) ( 93 ),經還原消除生成目標產物和Ni ( I )物種( 94 )。從[ CF3 OME BP H] *到(94)的SET給出了(91)和CF3-OME-BP。
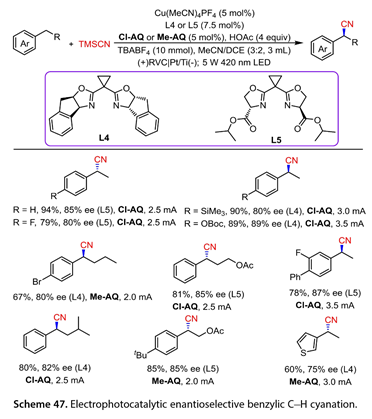
圖46 提出的交叉親電耦合機理
12.芐位C-H氰化
2022年,Liu課題組[32]報道了一種結合電光化學氧化和銅催化的高效的芐位C-H氰基化方法(圖47)。優化的反應條件為:420 nm LEDs照射,Cu(MeCN)4PF4 ( 5mol % ),雙惡唑啉( L4 / L5 , 7.5 mol %),2 -氯蒽醌( Cl-AQ )或2 -甲基蒽醌( Me-AQ ) ( 5mol % ),HOAc ( 4equiv ),TBABF4 ( 10 mmol )在MeCN / DCE中,以網狀玻碳( RVC )為陽極,Pt / Ti為催化劑,恒電流條件下反應在未分裂的細胞中的陰極。該反應有效地促進了芐位C-H的不對稱氰基化反應。對位被吸電子或富電子基團取代的乙苯類化合物與TMSCN高效地反應,以良好至高產率和良好的對映選擇性得到目標產物。鹵代正丁基苯以67 %的產率和80 %的ee值反應。含有OAc基團的底物以81 %的產率和85 %的ee值反應。異戊基苯和4 - (叔丁基)乙酸苯乙酯得到所需的手性產物(收率80 ~ 85 % , ee 82 ~ 85 %)。3 -乙基噻吩是這種不對稱芐位C-H氰化反應的良好底物。
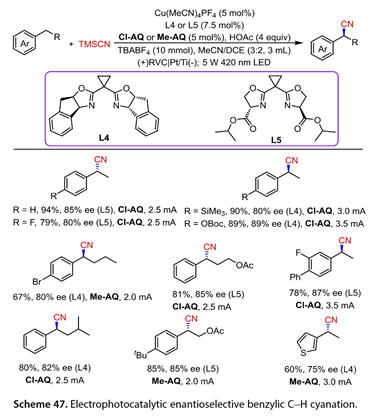
圖47. 電光催化對映選擇性芐位C-H氰化反應
激發態的R-AQ從乙苯中抽提一個氫原子,得到芐基自由基( 95 )和[R-AQ-H] * (圖 48 )。然后,L * Cu ( II ) ( CN )2 ( 97 )與(95)結合,得到目標分子和L * Cu ( I ) ( CN ) ( 96 )。[ R-AQ-H]*和(96)被陽極氧化,并伴隨著H2的析出完成催化循環。
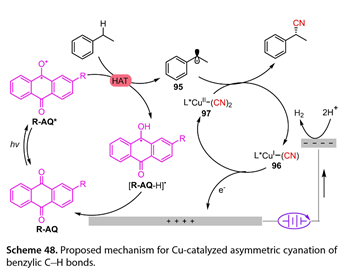
圖48. 提出了Cu催化芐位C氫鍵不對稱氰基化反應的機理
同年,Xu和合作者發展了一種無氧化劑的光電催化芐位C(sp3)-H不對稱氰基化制備手性芐腈的方法。這些作者提出了不同的機制( 圖 49 )。烷基芳烴可以向激發態光催化劑蒽醌- 2,7 -二磺酸鈉( AQDS * )轉移一個電子,產生離子-自由基對,該自由基對發生質子轉移,生成芐基自由基( 98 )和[ AQDS H ] *。然后,這個自由基( 98 )被L * Cu ( II ) ( CN ) 2 ( 99 )截獲,得到一個Cu ( III )物種( 100 ),它經過簡單的還原消除生成所需的手性芐腈和L * Cu ( I ) ( CN ) ( 101 )。最后,[ AQDS H ] *和(101)在陽極被氧化得到AQDS和(99)。
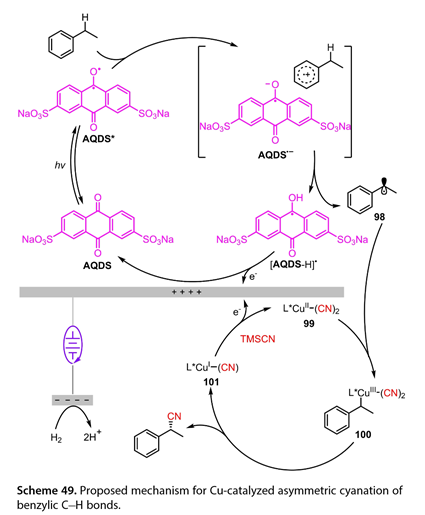
圖49. 提出了Cu催化芐基碳氫鍵不對稱氰化的機理
395 nm LEDs照射和同時電解的條件下,一系列官能化的烷基苯以較好的產率和較高的位點和對映選擇性發生反應( 圖 50 )。含有溴代物、磺酸鹽、環氧化合物、硅醚、酯、羧酸、烷基疊氮和氨基酯的乙苯進行芐位C(sp3)-H氰基化反應,產率為44 - 86 %。電子中性、富電子和缺電子的對位或間位取代的乙苯也產生了所需的產物( 51 ~ 84 %收率, 84 ~ 94 % ee)。5 -乙基- 2 -甲基吡啶與TMSCN的交叉偶聯反應以60 %的收率得到氰基化產物,ee值為81 %。具有多個潛在位點的底物以良好的產率和較高的位點選擇性和對映選擇性進行反應。較大的站點電子密度和較低的空間位阻是選擇性氰基化的首選。
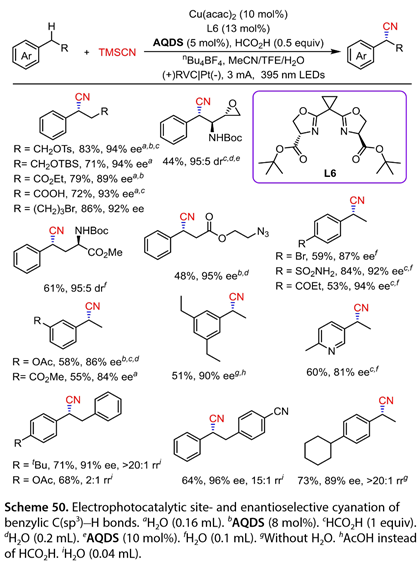
圖50. 芐基C(sp3)-H的電光催化位點和對映選擇性氰化
13.C(sp3)-H疊氮化
2020年,Lei課題組[34]報道了在電光催化條件下,以親核試劑NaN3為疊氮源,錳催化C(sp3)-H的氧化疊氮化反應(圖51)。在乙腈/乙酸混合溶劑中,1,10 -鄰菲羅啉(鄰菲羅啉, 20mol %),9 -芴酮( FLN為11mol %)或2,3 -二氯- 5,6 -二氰基對苯醌( DDQ , 5.5mol %),MnF2或MnBr2·4H2O ( 10 mol % ),KBr ( 40 mol % ),TFA ( 4.0 equiv )和LiClO4 ( 2.0 equiv )存在下,通過恒電流電解,在藍光LEDs照射下,可以容忍一系列芐基C(sp3)-H。三級芐基C(sp3)-H以良好的產率提供了預期的疊氮化產物。含有兩個三級芐基C(sp3)-H基團的1,4 -二異丙基苯可以以57 %的收率被使用,但得到了一些二疊氮化產物。乙苯衍生物與Na N3反應,以中等收率得到目標產物。一些含有簡單C(sp3)-H的未活化底物也能以31 - 50 %的產率得到C(sp3)-H疊氮化產物。在圖52中展示了這種C(sp3)-H的電光催化疊氮化的可能機理。在藍光LED的照射下,羰基可以達到其激發態,從而將一個氫原子從基底上抽離出來給出了C(sp3)自由基( 102 )和酮基自由基。后者在陽極被氧化以達到其基態。同時,NaN3將一個電子轉移到陽極,導致疊氮自由基的形成。隨后,疊氮自由基從底物中抽提H原子得到HN3和(102)。陽極與Mn (Ⅱ) ( N3 ) / L ( 104 )的SET反應得到Mn (Ⅲ) ( N3 ) / L ( 105 ),(102)與(105)反應得到預期產物和Mn (Ⅱ) / L ( 103 )。
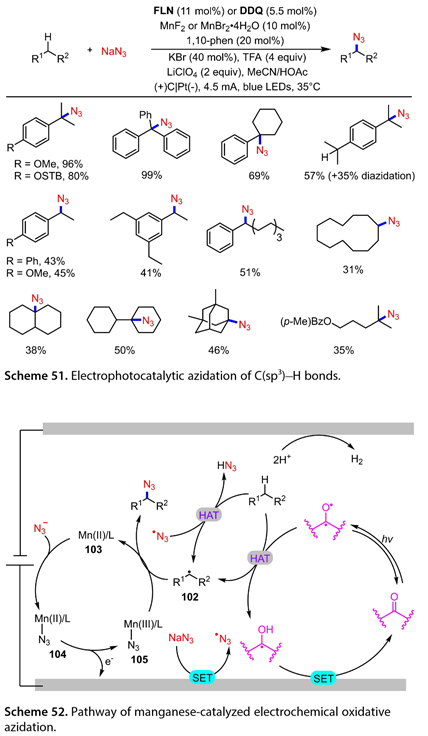
圖51和52. C(sp3)-H的電光催化疊氮化反應過程和機理
14.脂肪族的脫氫
Huang和他的合作者[35]報道了鈷催化的脂肪族底物的無受體脫氫反應( 圖 53 ),在DCE中使用2 -氯蒽- 9,10 -二酮( Cl-AQ , 25mol %)和dmgH2 ( 50 mol % )在400 - 415 nm的LED照射下進行。各種取代的乙苯是合適的底物,提供了71 - 95 %的預期脫氫產物的產率。2 -萘乙烷是可行的該反應的底物。四氫萘和環己基苯以32 - 67 %的收率轉化為萘和1,1'-聯苯。3 -苯甲酸苯丙酯反應,收率59 % ( E / Z = 1∶1)。硫醚,如乙基(萘- 2基)硫烷和2 - (苯乙硫基)嘧啶,順利地進行了脫氫反應(收率68 ~ 71 %)。N-芳基酰胺的反應以45 - 90 %的產率生成目標產物。有趣的是,α,β,γ,δ -不飽和內酰胺發生雙脫氫反應得到1 -苯基氮雜環庚- 2 -酮。使用1,2,3,4 -四氫萘- 2 -醇或4 -苯基環己- 1 -醇得到了目標產物(收率61 ~ 96 %)。3 -苯基丙酸苯酯以42 %的收率( E / Z = 1∶1.2)脫氫。
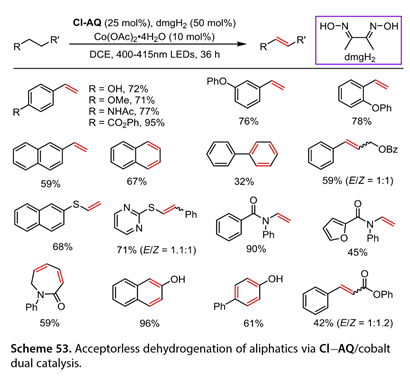
圖53. 通過Cl-AQ /鈷雙催化實現脂肪烴的無受體脫氫
該催化脂肪底物脫氫反應的詳細機理如圖54所示。激發態的Cl-AQ ( Cl-AQ * )與脂肪族底物之間的HAT可以得到烷基自由基( 106 )和[ Cl-AQ-H] *。前者被鈷肟配合物( 107 )捕獲,得到[ CoⅢ] -烷基化合物( 108 )。隨后,在光照下,108可以發生均裂[ CoⅢ] -烷基鍵的均裂和鈷介導的β - H原子抽提,生成目標產物和Co (Ⅲ)氫化物( 109 )。生成的(109)隨后氧化[ Cl-AQ-H] *形成Co ( II ) H ( 110 )和質子化的Cl-AQ ( 111 )。最后,(111)足夠酸性質子化(110)生成(107)和Cl-AQ,同時釋放H2,從而完成催化循環。
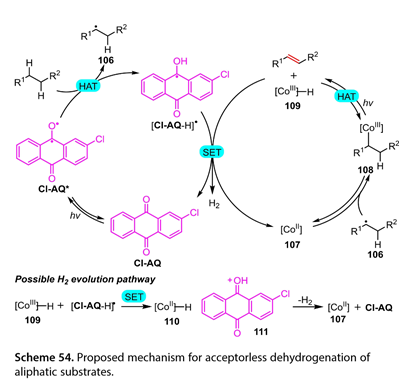
圖54. 提出了脂肪族底物無受體脫氫的機理
15. C(sp3)-H氧雜環的官能化
Kong課題組[36]公開了一種利用( 4 -甲氧基苯基) ( 4- (三氟甲基)苯基)甲酮( CF3-OME-BP)和鎳雙催化體系,在10 W 390 nm LEDs照射下對氧雜環進行對映選擇性C(sp3)-H官能化的方法( 圖 55 )。芳基溴化物與酯或對位苯環上的氟反應,以67 - 75 %的產率和88 - 90 %的ee值得到目標產物。電子中性的芳基溴化物4 -溴- 1,1 ' -聯苯也能以61 %的產率得到88 %的ee值。4 -溴- 2 -氯- 1 -氟苯與四氫呋喃反應得到了69 %的產率和88 %的ee值。
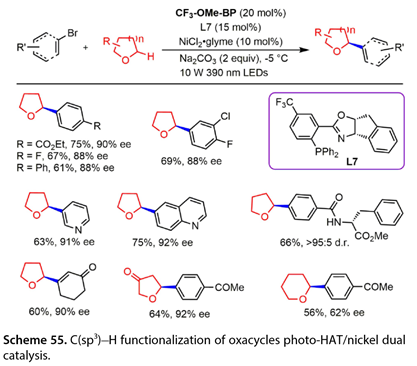
圖55. 氧雜環C(sp3)-H官能化的光- HAT /鎳雙催化
該光催化反應與3 -溴吡啶或6 -溴喹啉的光催化反應同樣成功,產率為63 - 75 % ( 91 ~ 92 % ee)。一個復雜分子衍生的芳基溴化物是該反應的活性底物。用四氫呋喃處理活化的烯基溴化物,如3 -溴環己- 2 -烯- 1 -酮,以60 %的產率和90 %的ee值得到了預期的產物。最后,使用四氫呋喃- 3 -酮和氧雜環己烷分別以64 % ( 92 % ee )和56 % ( 62 % ee )的產率得到相應的產物。
基于密度泛函理論計算,發展了一種可能的機理( 圖 56 )。用10 W 390 nm的LED照射CF3-OME-BP形成的激發態CF3-OME-BP ( CF3-OME-BP*),可以提取無水乙醇。H原子從四氫呋喃中生成以碳為中心的自由基( 112 )和[CF3-OME-BP-H] *。L-NiII-Cl2 ( 113 )再氧化[CF3-OME-BP-H] *得到[CF3-OME-BP]和L - NiI-Cl ( 114 )。中間體(114)可以捕獲(112)生成Ni ( II )(115)。(115)和[ CF3-OME-BP-H] *之間的SET導致形成Ni ( I ) (116),并再生CF3-OME-BP。1- ( 4 -溴苯基)乙酮氧化加成(116)得到Ni ( III )(117),再經還原消除得到目標產物和L - NiI-Br ( 118 )。
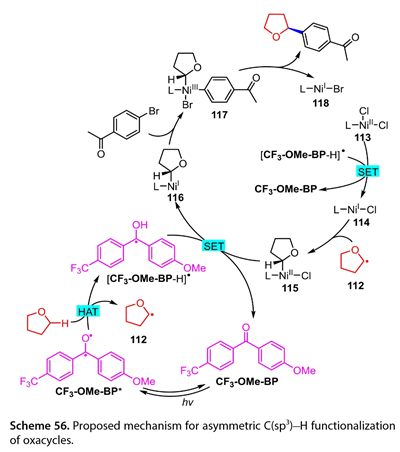
圖56. 提出了惡環不對稱C(sp3)-H官能化的機理
16.α -氨基C(sp3)-H的烷基化
2021年,Vincent和圖萊克等人[37]報道了Cu (Ⅱ)配合物( CuⅡ- 1 )催化的N -烷基苯胺的直接C(sp3)-H烷基化反應,該反應結合了銅催化劑和二苯甲酮光催化劑( 圖57 )。在365 nm光照下,丙烯酸酯、4 -乙烯基吡啶和環己- 2 -烯- 1 -酮等一系列Michael受體與N,N -二甲基苯胺反應,得到了一系列的烴基化產物(收率46 ~ 91 %)。4 -位含氰基或甲基的N,N -二甲基苯胺與丙烯酸乙酯反應可以以80 - 92 %的產率得到目標產物。值得注意的是,N,N -二甲基吡啶- 4 -胺的反應產率為56 %。用CN基團或1 -苯基哌啶取代N -甲基苯胺,以45 - 71 %的收率得到目標產物。
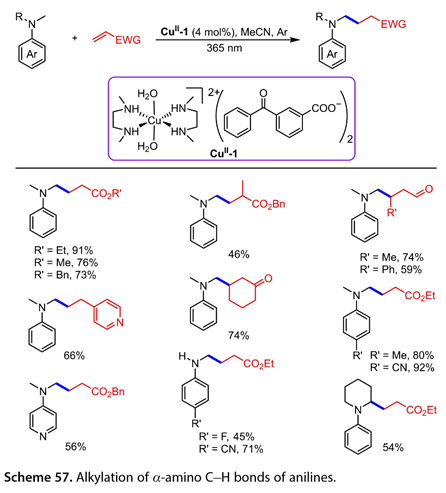
圖57. 苯胺的α -氨基C-H鍵的烷基化
我們提出了N -烷基苯胺直接C(sp3)-H烷基化反應的機理( 圖 58 )。激發態的BPCO2 ( 3BPCO2 )可以氧化苯胺得到[ BPCO2 ] *和苯胺自由基陽離子( 119 )。(119)和[ BPCO2 ] *之間的質子轉移產生自由基( 120 )和[ BPHCO2 ] *。隨后,(120)被烯烴捕獲得到親電自由基( 121 )。同時,[ BPCO2 ] *或[ BPHCO2 ] *可以將CuⅡ或CuⅠ物種還原為CuⅠ或Cu0,同時再生BPCO2的基態。前者與(121)反應,生成目標產物。
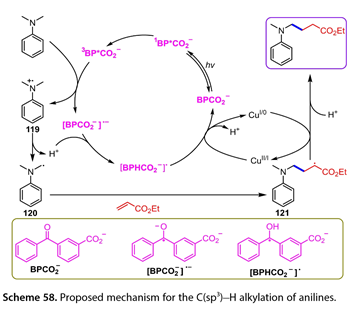
圖58. 提出了苯胺的C(sp3)-H烷基化反應機理
17.總結與展望
本文綜述了近年來羰基-光氧化還原/金屬雙催化體系在構建碳-碳鍵和碳-雜原子鍵方面的研究進展。羰基光催化劑有效地充當了單電子反式-Fer試劑,能量轉移試劑或氫原子轉移試劑促進金屬催化的酰化,硼化,環化,磺酰化,芐位C-H三氟甲基化,炔基化,膦酰化,芳基鹵化物的酯化和醚化,脂肪烴的脫氫,氧雜環的C(sp3)-H官能化,α-氨基C-H鍵的烷基化,烯烴的氫酰化和三組分烯烴加成。特別值得注意的是,發展了C(sp3)-H的疊氮化或不對稱芐位C-H氰化的方法,涉及電光化學氧化和銅/錳催化的組合。盡管在該領域已經取得了許多進展,但仍然存在一些挑戰,包括開發新的、高效的光催化劑、改造更具挑戰性的偶聯伙伴、立體選擇性不對稱反應、使用環境友好的溶劑和合成先進的藥物成分。我們預期,羰基-光氧化還原/金屬雙催化將成為一種通用的、高效的策略,在實驗室和工業規模上構建復雜分子具有廣泛的吸引力。








 客服QQ
客服QQ